آزمایش ژنتیک چیست
مدیر سایت
پنج شنبه, 27 آبان 1400 11:00
مواد معدنی و نقش آن ها در بدن انسان
به مواد معدنی ابزار بدن گفته می شود، برای تمام فعالیت های بیوشیمیایی مانند تولید آنزیم ها، هورمون ها، تولید انرژی و به طور کلی برای فعالیت تمام بخش های بدن مورد استفاده قرار می گیرند، به عنوان مثال بدن از عنصر روی برای تولید بیش از 100 آنزیم از جمله آنزیم های گوارشی، تولید پروتئین، تبدیل مواد غذایی به انرژی، تولید اسپرم و غیره، از کلسیم برای تولید ناقل های شیمیایی بین سلولی، تبدیل چربی به انرژی و برای ترمیم استخوان ها و دندان ها، از آهن برای تولید گلبول های قرمز خون، از منیزیم برای تنظیم ضربان قلب و فشار خون، تولید ATP، تولید بیش از 400 آنزیم و غیره استفاده می نماید. به عبارتی هر یک از مواد معدنی نقش های متعددی در بدن ایفا می نمایند که به طور مختصر به برخی اشاره شد. بسیاری از بیماری ها و مشکلات ارتباط مستقیم با عدم توازن میزان مواد معدنی در بدن دارند که در ادامه این مقاله درباره آن بیشتر صحبت خواهیم کرد

مواد معدنی را می توان به 3 دسته تقسیم نمود:
1. مواد معدنی ماکرو(اصلی): به مواد معدنی گفته می شود که بدن به میزان زیادی از آن ها نیاز دارد و شامل: کلسیم، منیزیم، سدیم، پتاسیم، فسفر و گوگرد می باشد.
2. مواد معدنی کمیاب: که بدن به میزان کم جهت متابولیزم و انجام فعالیت های بیوشیمیایی به آن ها نیاز دارد و شامل: آهن، منگنز، مس، روی، کروم، سلنیوم، ید و غیره می باشد.
3. فلزات سمی: موادی معدنی می باشند که هیچ نقش مفیدی در بدن ایفا نمی کنند و با جایگزین شدن به جای مواد معدنی مفید سبب اختلال در متابولیزم و فعالیت بخش ها، اندام ها و بروز بیماری ها و حتی مشکلات ژنتیکی می گردند. امروزه به دلیل آلودگی محیط زیست انسان با بیشترین حجم این مواد در طول تاریخ مواجه است. این فلزات عبارتند از: جیوه، سرب، آرسنیک، کادمیوم، آلومینیوم و تعدادی دیگر.
منتشرشده در
مقالات
برچسبها
پنج شنبه, 27 آبان 1400 11:00
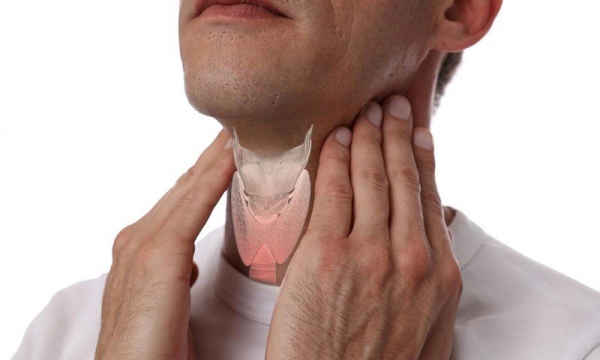
آیا بیماری هاشیموتو در دوران بارداری مشکل ایجاد میکند؟
بیماری هاشیموتو در دوران بارداری : بدون درمان، کم کاری تیروئید میتواند برای مادر و کودک مشکل ایجاد کند. با این حال، داروهای تیروئید میتوانند به پیشگیری از بروز مشکلات کمک کرده و مصرف آنها در دوران بارداری خطرناک نیست. علاوه بر این، زنانی که داروهای تیروئید مصرف میکنند، در دوران بارداری ممکن است نیاز به دوز بیشتری داشته باشند. بنابراین، اگر باردار شدید، با پزشک خود تماس بگیرید.
علائم هاشیموتو
در ابتدا، بسیاری از افراد مبتلا به این بیماری هیچ علائمی ندارند. با پیشرفت بیماری، غده تیروئید معمولا بزرگتر شده و ممکن است منجر به تورم گردن شود. بزرگ شدن غده تیروئید را گواتر مینامند. با پیشرفت کم کاری تیروئید، ممکن است علائم زیر ظاهر شوند:
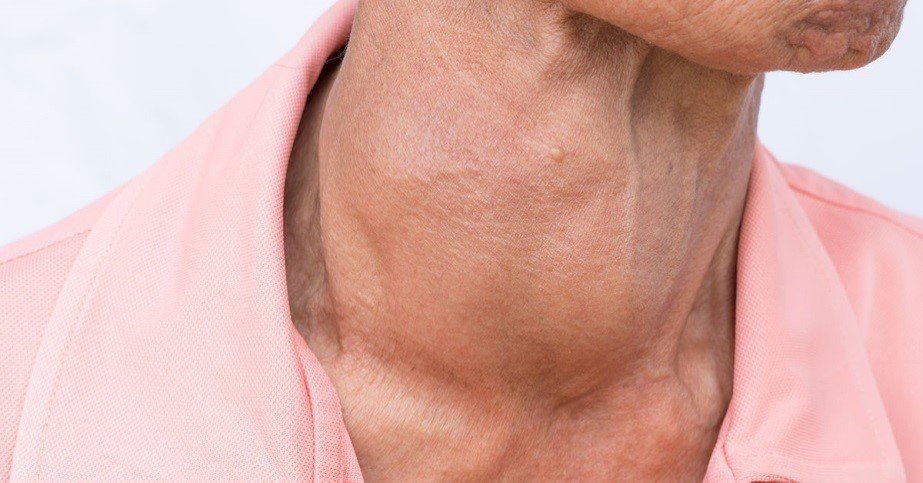
خستگی
افزایش وزن
عدم تحمل سرما
درد مفصل و عضلات
یبوست
خشک شدن و نازک شدن موها
نامنظم شدن دورههای قاعدگی و بروز مشکلات مرتبط با بارداری
افسردگی
مشکلات حافظه
کاهش ضربان قلب
منتشرشده در
مقالات
برچسبها
پنج شنبه, 27 آبان 1400 10:48
جداسازی DNA های حلقوی از باکتری ها ( استخراج پلاسمید )
هدف: جداسازی DNA های حلقوی از باکتری ها ( استخراج پلاسمید )
دامنه کاربرد: کلونینگ، بررسی قطعات ژنی
این تکنیک همانند استخراج DNA می باشد با این تفاوت که در استخراج پلاسمید لازم است که DNA ی پلاسمیدی از مقدار زیادی DNA ی کروموزومی که در سلولهای باکتریائی موجود است مجزا شود. جداسازی دو DNA از یکدیگر مشکل است که روشهای متعددی برای حذف DNA ی باکتریائی طی خالص کردن پلاسمید وجود دارد.
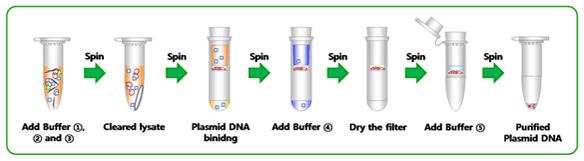
در این تکنیک مرحله ای که باعث شروع فرآیند میشود این است که باید باکتری ها را لیز کنیم و با تغییر PH سبب دناتوره شدن DNA ژنومیِ ( کروموزوم اصلیِ) باکتری شویم ولی پلاسمیدها دناتوره نمی شوند.
در مرحله ی بعد با خنثی کردن PH سبب Clot شدن و رسوب DNA کروموزوم اصلی می شویم ولی پلاسمیدها همچنان محلول هستند.
در مرحله ی آخر میتوان با استفاده از فیلتر سبب رسوب پلاسمیدها روی فیلتر شویم و با کمک آب دیونیزه پلاسمیدها را از روی فیلتر جداسازی کنیم.
آزمایشات تخصصی همه روزه در آرمایشگاه ایراژن انجام میگردد.
منتشرشده در
مقالات
برچسبها
پنج شنبه, 27 آبان 1400 10:48
ميزان نرمال TSH در باردارى
ميزان نرمال TSH در باردارى بر اساس گايدلاين كشورى:
– در تريمستر اول ٠/٢-٣/٩
– در تريمستر دوم ٠/٥-٤/١
– و در تريمستر سوم ٠/٦- ٤/١ ميباشد،
كه با مقاديرى كه اينترنشنال معرفى شده متفاوت است.
بهتر است براى هر خانمى كه تمايل به باردارى دارد و يا در اولين ويزيت باردارى TSH چك شود و در صورتى كه بالاى ١٠ بود حتماً درمان شروع شود
و در صورتى كه بين ٣/٩ و ١٠ در تريمستر اول و يا ٤/١ و ١٠ در تريمستر دوم و سوم بود ابتدا آنتى TPO و T4 چك و در صورت مثبت بودن TPO با هر تيترى و يا پايين بودن T4 كمتر از ٧/٥ درمان با لووتيروكسين شروع شود و رنج نرمال T4 در باردارى ٧/٥ – ١٨ در نظر گرفته ميشود.

چك TSH از ٨ صبح تا ٦ عصر بدون نياز به ناشتا بودن قابل انجام است و نياز به قطع قرص لووتيروكسين نميباشد ولى در صورت لزوم چك T3 ,T4 ,T3ru صبح روز آزمايش قرص مصرف نشود و بعد از خونگيرى قرص مصرف شود.
اگر بيمار ساب كلينيكال بود (حد فاصل مقاديرى كه ذكر شد تا ١۰) و TPO و T4 نرمال بود درمان صورت نميگيرد ولى هر ٤ هفته تا نيمه باردارى و يكبار هم بين هفته ٢٦ تا ٣٢ TSH چك ميشود.
در صورت مثبت بودن TPO و يوتيروئيد بودن نيز درمان انجام نميشود ولى فالو با روش ذكر شده در بالا انجام ميگيرد.
ميزان يد مورد نياز در باردارى و شيردهى به ترتيب ٢٥٠ و ٣٠٠ ميباشد كه با رژيم غذايى در نهايت ١٥٠ ميكرو قابل تأمين است و بقيه بايد با مكمل تأمين شود كه قبل باردارى و سه ماه اول يدوفوليك و در سه ماهه دوم و سوم و شيردهى مكمل هاى حاوى يد توصيه ميشود.
مقادیر TSH در بارداری طبق ویلیامز 2014:
در زمان غیر بارداری: 4.25_0.34
تریمستر اول: 3.40_0.6
تریمستر دوم: 3.60_0.37
تریمستر سوم: 4.04_0.38
منتشرشده در
مقالات
برچسبها
پنج شنبه, 20 آبان 1400 10:25
اندازه گیری الکترولیت های ادرار در آزمایشگاه
آزمایش الکترولیت ادرار در آزمایشگاه
اندازه گیری الکترولیتهای ادراری تفاوتی با سایر مایعات بدن نداشته و تنها عدم استفاده از مواد نگه دارنده در نمونه ها بوده و همان شرایطی را که در سایر مایعات رعایت می شوند در این مورد نیز بایستی مد نظر قرار گیرند .
بعنوان مثال از آنجایی که پتاسیم یک آنیون داخل سلولی است در صورت وجود همولیز داخل عروقی و یا خارج عروقی گلبولهای قرمز یا هر نوع آسیب سلولی در تمام سطح بافتهای مختلف بدن از جمله قلب و خود سلولهای کلیه باعث افزایش آنها خواهد شد لذا توجه به این نکات حائز اهمیت است.
از سوی دیگر از آنجایی که بهترین و در دسترس ترین روش معرفی شده برای اندازه گیری الکترولیتهایی مانند سدیم، پتاسیم، و لیتیم فلیم فتومتری است. و گزارشات فلیم فتومتری بصورت میلی اکی والان در لیتر بیان می شود، بایستی پس از بدست آوردن مقدار این یونها در حجم ادرار ۲۴ ساعته به لیتر ضرب گردد تا مقدار تام سدیم و پتاسیم دفعی در ۲۴ ساعت بدست آید.
در صورتی که نمونه در یخچال نگه داری گردد میزان مقادیر سدیم و پتاسیم نسبتا پایدار بوده و مقادیر نرمال بخصوص میزان سدیم ادرار به مقدار مصرف این یون به عنوان مثال مصرف نمک بستگی دارد.
مقادیر نرمال سدیم در فردی که به مقدار نرمال نمک مصرف می کند در ادرار ۲۴ ساعته در حدود:۲۲۰-۴۰ میلی اکی والان در لیتر گزارش شده است.
مقدار نرمال پتاسیم نیز تابع مصرف غذایی بوده ولی لزوما همبستگی و تناسب خاصی ندارد و میزان نرمال آن ۱۲۵-۲۵ میلی اکی والان در ادرار ۲۴ ساعته است.
منتشرشده در
مقالات
برچسبها
پنج شنبه, 20 آبان 1400 10:25
ورم معده
ورم معده چیست ؟
ورم معده یا گاستریت به التهاب دیواره معده گفته می شود. علل بروز این عارضه ضعف در مخاط پوششی دیواره معده می باشد . این مخاط وظیفه حفاظت از دیواره معده را به عهده دارد و در صورت اختلال در کار آنها آنزیم های گوارشی فرصت تخریب دیواره معده را پیدا می کنند که نتیجه آن التهاب در دیواره معده می باشد. ناگفته نماند از جمله عوارض برخی از بیماری های می تواند ورم معده باشد. گاستریت بر دو نوع حاد و مزمن می باشد. همچنین این عارضه می تواند سبب زخم معده و یا افزایش خطر ابتلا به سرطان معده باشد. خوشبختانه در اکثر اوقات ورم معده خیلی جدی نبوده و به سرعت قابل درمان می باشد.
علل گاستریت :
- عفونت های باکتریایی : یکی از شایع ترین عفونت های دنیا ابتلا به عفونت هلیکوباکتر پیلوری می باشد به گونه ای که شاید به توان گفت همه افراد جهان به آن مبتلا می باشند .
- افراط در استفاده از مسکن ها : استفاده مداوم از مسکن ها سبب از بین رفتن ماده کلیدی محافظ معده می شود.
- افزایش سن : افراد مسن بیش از بقیه افراد مستعد گاستریت می باشند زیرا پوشش محافظ معده با افزایش سن نازک می گردد از دیگر دلایل می توان به افزایش احتمال اختلالات ایمنی و عفونت هیلکوباکتر پیلوری با افزایش سن اشاره نمود .
- مصرف مشروبات الکلی : الکل سبب تحریک پوشش معده به آنزیم های گوارشی می گردد.
- استرس : استرس سبب ابتلا به گاستریت حاد می گردد.
- حمله سیستم ایمنی بدن: در این حالت سیستم ایمنی بدن به حافظ معده حمله کرده و سبب از بین رفتن آن می شود.
- برخی بیماری ها : مانند ایدز، کرون، عفونت های انگلی و …
پیشگیری :
با تغییر در شیوه زندگی و رژیم غذایی مناسب ، با شستن مرتب دست ها با آب و صابون می توان از ابتلا به این میکروب جلوگیری به عمل آورد.
آزمایشات مربوطه :
شاید بتوان گفت پیشگیری از ورم معده برابر با پیشگیری از میکروب هلیکوباکترپیلوری می باشد زیرا یکی از مهمترین عاملان تشکیل آن میکروب هیلکوباکتر پیلوری می باشد . آزمایش هلیکوباکتر پیلوری IgG ، IgM، IgA در خون و همچنین میکروب هلیکوباکترپیلوری در مدفوع و یا تست تنفسی UBT راه هایی برای تشخیص میکروب هلیکو باکتر می باشند . لازم به ذکر است آزمایشات خون و مدفوع فاقد نیاز به شرایط خاص می باشند اما تست تنفسی بر خلاف آنان نیاز به ناشتایی و عدم استفاده از داروهای معده در حداقل یک هفته مانده به انجام آزمایش دارد.
منتشرشده در
مقالات
برچسبها
یکشنبه, 16 آبان 1400 12:55
تست آلفافتوپروتئين
تست AFP مخفف Alpha-fetoprotein (آلفافیتوپروتئین) است
این تست نیاز به آمادگی خاصی ندارد و نمونه مورد نظر سرم فرد می باشد.
پزشک زمانی این تست را در درخواست می كند که فرد مشكوك است که سرطان کبد یا سرطان های خاص بیضه یا تخمدان دارد؛ بیمار مبتلا به بیماری مزمن کبدی را از نظر ظهور كارسينوماي هپاتوسلولار و یا نوع دیگری از سرطان کبد پايش مي كند؛ اثربخشی درمان در بیمار مبتلا به سرطان کبد، بیضه یا تخمدان را پايش مي كند؛ عود سرطان را پايش مي كند.
البته گاهی اوقات وقتي بيمار هپاتیت مزمن یا سیروز دارد درخواست مي شود.
این تست مقدار آلفا فتوپروتئین (AFP) را در خون اندازه گیری مي كند. AFP، پروتئیني است كه عمدتا توسط کبد جنین و بخشی از جنین در حال رشد که شبیه به حفره زرده در تخم پرندگان است (بافت هاي کیسه زرده) تولید می شود. غلظت AFP بطور شاخص هنگامی که نوزاد متولد می شود، افزايش مي يابد و پس از آن به سرعت کاهش مي يابد. در کودکان سالم و بالغین غیرباردار به طور طبيعي فقط در سطوح بسیار پایین قابل تشخیص است.
شرایط افزایش میزان AFP :
آسیب کبدی و بعضی سرطان ها (سرطان تخمدان و تومور سلول زاياي بیضه) می توانند غلظت AFP را به طور قابل توجهی افزایش دهند. سطوح بالای AFP ممکن است گاهی اوقات با سرطان های دیگر مانند معده، روده بزرگ، ریه، پستان و لنفوم دیده شود. هر زمان که سلول های کبدی بازسازی مي شوند، AFP تولید مي شود. AFP در بیماری های مزمن کبدی، مانند هپاتیت و سیروز ممکن است براي مدت طولاني افزایش يابد. غلظت های بسیار بالا از AFP ممکن است توسط تومورهاي خاص تولید شود.
از آنجا که AFP در جنین تولید می شود، سطح آن معمولا در زنان باردار و نوزادان بالاتر است.
شرایط کاهش میزان AFP :
وقتی AFP به عنوان ابزار پايش استفاده می شود، کاهش آن پاسخ به درمان را نشان می دهد.
منتشرشده در
مقالات
برچسبها
یکشنبه, 16 آبان 1400 12:47
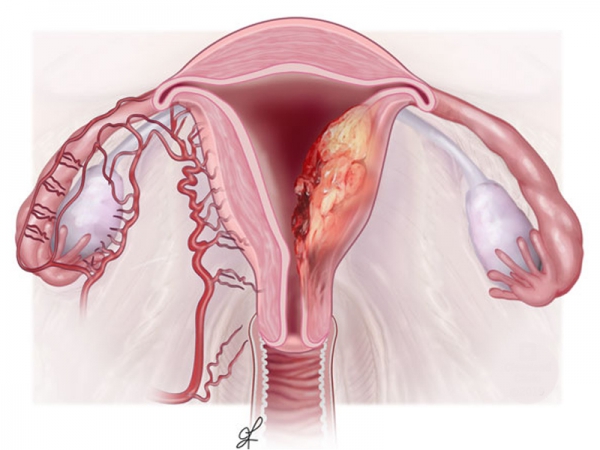
سرطان رحم
در ابتدای شروع سرطان رحم در بدن نشانهای بروز نمیکند.
ولی نشانههای بعدی این بیماری میتواند شامل خونریزی واژنی، درد لگن یا دیسپارونیا (به هرگونه فعاليت جنسی که همراه با درد باشد، ديسپارونيا يا فعاليت زناشويی دردناک گويند.) باشد.
سرطان رحم معمولاً به دنبال تغییرات پیشسرطانی، در مدتی بیش از ده تا بیست سال پیشرفت میکند.
در سراسر دنیا سرطان دهانه رحم چهارمین عامل مرگ زنانی است که بر اثر سرطان از بین میروند.
علت بروز سرطان رحم چیست؟
در ۹۰ درصد موارد، این بیماری به علت عفونت ویروس پاپیلومای انسانی (HPV) ایجاد میشود.
هنگامی که این ویروس برای چند سال در بدن باقی میماند، به تدریج برخی از سلولها را در گردن رحم به سلولهای سرطانی بدل میکند و این سلولها به طور پیشرونده مهاجمتر میشوند.
انواع سرطان رحم ؟
حدود نود درصد از آن شامل کارسینوم سلول-سنگفرشی (به رشد بدخیم سلولهای پوششی در هر اندامی که میتواند به بافتهای اطراف نفوذ کرده و توانایی متاستاز داشته باشد، کارسینوم گفته میشود.)
ده درصد آدنوکارسینوم (به سرطان در بافت غدد آدنوکارسینوم گفته میشود) و تعداد کمی شامل موارد دیگر میشود.
عوامل ریسک سرطان رحم ؟
- ویروس پاپیلوس انسانی (HPV)
در اینجا صدها ویروس مختلف جمع شدهاست. برخی از آنها از طریق تماس پوستی منتقل میشوند و پیش زمینهی سرطان دهانه رحم محسوب میشوند.
شناسایی HPV معمولا از طریق یافتن زیگیلها یا آزمایش پاپ اسمیر انجام میشود.
- قرصهای ضد بارداری
هورمونهای زنانهای که در برخی داروهای ضد بارداری خوراکی یافت میشود شاید برای برخی سرطانها بهترین زمینهی گسترش را فراهم میکند.
همچنین هر چه زن مدت طولانیتری داروی ضد بارداری خوراکی مصرف کند ریسک ابتلا به سرطان دهانه رحم در او بالاتر میرود و بعد از ۵ سال مصرف ۲ برابر میشود.
ژنتیک
دربارهی این موضوع منابع متناقضی وجود دارد. برخی منابع ادعا میکنند سرطان دهانه رحم چیزی است که در بین اعضای خانواده به ارث میرسد.
زنانی که سابقهی ژنتیکی دارند ۲-۳ برابر بیشتر در معرض خطر سرطان هستند. با این حال من منابع دیگری دیدهام که ادعا میکنند در این نوع سرطان مولفهی ژنتیک تاثیری ندارد.
- ۴. HIV
ویروسی که سبب ایدز میشود به سیستم ایمنی آسیب میزند و خطر عفونت HPV را افزایش میدهد. - عفونت کلامیدیا
در زنانی که قبلا یا اکنون نشانههای عفونت کلامیدیا در آنها مشاهده شدهاست خطر ابتلا به سرطان رحم بالاتر است. - مصرف دخانیات
زنانی که دخانیات مصرف میکنند خطر ابتلا به سرطان دهانه رحم را در خودشان ۲ برابر میکنند. این باور وجود دارد که محصولات جانبی تنباکو به DNA سلولهای دهانهی رحم آسیب میزند، و ممکن است در پیشرفت این سرطان نیز موثر باشد. مصرف دخانیات روی سیستم ایمنی نیز تاثیر میگذارد، و مبارزه با عفونت HPV را دشوارتر میکند. و در واقع مصرف دخانیات یکی از ۱۰ عادتی است که اگر میخواهید سلامت باشید باید همین حالا ترک کنید. - چندین بارداری
زنانی که ۳ بار یا بیشتر بارداری کامل داشتهاند بیشتر در معرض خطر ابتلا به سرطان دهانه رحم هستند. هیچ کس واقعا نمیداند چرا اینطور است. - نخستین بارداری در سن پایین
زنانی که در زمان نخستین بارداری کامل کمتر از ۱۷ سال سن داشتهاند تقریبا ۲ برابر بیشتر از زنانی که برای بارداری تا ۲۵ سالگی یا بیشتر صبر کردهاند احتمال دارد بعدها در زندگی به سرطان دهانه رحم مبتلا شوند.
درمان سرطان رحم ؟
مرحله (شدت) سرطان را تعیین کنید
مراحل پیشرفت سرطان دهانه رحم از مرحله صفر تا مرحله چهار است.
طبقه بندی به سه عامل بستگی دارد: میزان تومور اصلی، اگر سرطان به غدد لنفاوی اطراف گسترش یافته و اینکه آیا سرطان به قسمت های دور بدن شما گسترش یافته است یا خیر.
پزشک شما مرحله ابتلا به سرطان را ارزیابی می کند و بر اساس آن گزینه های درمان را ارائه می دهد.
مرحله صفر: سلول های سرطانی بر روی سطح گردن رحم یافت می شوند اما در بافت رشد نکرده اند. این مرحله همچنین کارسینوما در محل (CIS) نامیده می شود.
- مرحله اول: سلول های سرطانی به رحم رسیده اند، اما سرطان در خارج از رحم رشد نمی کند.
- مرحله دوم: سرطان به گردن رحم و رحم رسیده است، اما به دیواره های لگن یا بخش پایین تر از واژن نرسیده است
- مرحله سوم: سرطان به قسمت پایین واژن و یا دیواره های لگن گسترش یافته است و ممکن است حفره ها را مسدود کند. ممکن است به غدد لنفاوی در لگن، اما نه به قسمت های دور بدن شما گسترش یابد.
- مرحله چهارم: پیشرفته ترین مرحله سرطان که در آن سرطان گسترش یافته است (متاستاز) و به قسمت های دور بدن شما گسترش یافته است.
- درمان مرحله صفر سرطان با برداشتن سلول ها
علت سرطان رحم ؟
سرطان هر مرحله با بیوپسی مخروطی تأیید می شود، که روشی است که پزشک با ضایعه بر روی دهانه رحم را بر می دارد.
سپس آن را زیر میکروسکوپ بررسی می کند. مرحله ۰ را می توان با اقدامات جزئی جراحی مانند فریز کردن، برداشتن با لیزر و برداشتن با حلقه انجام داد.
معاینه میکروسکوپی تشخیص سرطان را تایید می کند و همچنین به پزشک شما اطلاع می دهد که آیا تمام سلول های سرطانی به طور موثر حذف شده اند یا خیر.
پس از درمان، شما نیاز به نظارت مادام العمر برای اطمینان از اینکه تمام سلول های سرطانی حذف شده اند واینکه سرطان بازگشت ندارد را دارید.
از دکتر خود بپرسید که آیا شما به درمان بیشتر نیاز دارید یا نه
اگر سرطان شما بسیار بزرگ است یا قبلا گسترش یافته است، قطعا باید به گزینه های درمان مراحل بعد برای سرطان دهانه رحم مراجعه کنید
با این حال، اگر سرطان شما به نظر می رسد که کوچک است و هنوز در دهانه رحم مانده است، تخلیه (حذف) ممکن است کافی باشد.
همه این ها به حاشیه ها بستگی دارد. این بدان معنی است که وقتی پزشک شما قطعه ای را که جدا شده بود را زیر میکروسکوپ بررسی می کند.
حاشیه ها (یا مرزها) بخش حذف شده را برای اطمینان از اینکه آنها بدون سرطان هستند، بررسی می کند.
اگر حاشیه ها بدون سرطان باشند، معمولا این بدان معنی است که کل سرطان حذف شده است. شما ممکن است نیاز به درمان بیشتر نداشته باشید.
اگر حاشیه حاوی سلول های سرطانی باشد، به این معنی است که سرطان به طور کامل درمان نشده است و شما باید با پزشک خود در مورد گزینه های درمان دیگر که در بخش بعدی این مقاله پوشش داده می شود صحبت کنید.
جراحی را انتخاب کنید.
منتشرشده در
مقالات
برچسبها
شنبه, 15 آبان 1400 13:22
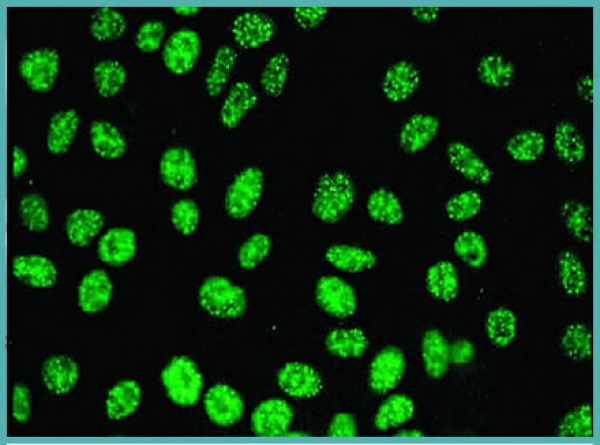
آزمایش AMA معروف به Mitochondrial Antibody
آزمایش AMA معروف به Mitochondrial Antibody ( آنتی بادی ضد میتوکندریال و آنتی بادی M2 ضد میتوکندریال )
تستهای مرتبط : ANCA ، ANA ، آنتی بادی میکروزومال کبد/کلیه ، آلکالین فسفاتاز ، آلانین آمینو ترانسفراز و SMA( آنتی بادی ماهیچه صاف ).
هدف انجام تست چیست؟
برای کمک به تشخیص PBC ( سیروز صفراوی اولیه ) انجام می شود.و هنگامی درخواست می شود که پزشک شما به PBC مشکوک باشد.
نمونه مورد نیاز چیست؟
نمونه خون گرفته شده از ورید برای این تست لازم است
آیا آزمایش نیاز به آمادگی دارد ؟
خیر
این تست چیست؟
این تست مقادیر آنتی بادیهای ضد میتوکندریال را در خون اندازه میگیرد.تولید مقادیر زیاد AMA رابطه قوی با بیماری PBC دارد. PBC اختلالی خود ایمن است که باعث التهاب و زخمهای مجاری صفراوی درون کبد میشود و باعث تخریب کبد و انسداد جریان صفراوی می شود.این بیماری به طور شایع در خانمهای بین سنین 35 الی 60 سال رایج است. حدود 90% افراد مبتلا به PBC دارای مقادیر واضحی از A.M.A هستند.
مقادیر افزایش یافته سطح A.M.A همچنین در کولانژیت اسکلروزه اولیه و ثانویه ، بیماری کبد مرتبط با بیماری التهابی روده مزمن (IBD) و همچنین انسداد مجاری صفراوی دیده می شود.علاوه بر این سطوح افزایش یافته سطح آلکالین فسفاتاز سرمی هم ممکن است مشاهده شود.
9 نوع آنتی ژن AMA ، (M1 – M9) وجود دارد که انواع M2 و M9 آن دارای اهمیت کلینیکال هستند. حضور نوع M2 به طور اختصاصی شاخص PBC می باشد در حالی که آنتی ژنهای دیگر در شرایط دیگری یافت می شوند.به طوری که امروزه بعضی آزمایشگاه ها از تست A.M.A-M2 به جای A.M.A استفاده می کنند.
تستهای دیگری که به کشف PBC و همچنین افتراق آن از دیگر بیماری های خود ایمن کمک می کنند عبارتند از :
Smooth muscle antibodies (SMA)
Antinuclear antibodies (ANA)
Alkaline phosphatase
IgM level
Bilirubin
Albumin
Prothrombin time
C-reactive protein
GGT
تفسیر نتایج چگونه است؟
زمانی که مقادیر مشخصی از AMA یا AMA-M2 در خون بیمار یافت می شود بیشترین علت ابتلا به PBC می باشد.
?مقادیر کم A.M.A در شرایط زیر یافت می شود :
عفونت هپاتیت فعال مزمن ، عفونت هپاتیت خودایمن و سیفلیس .
همچنین A.M.A ممکن است در اختلالات خود ایمنی مثل SLE ، آرتریت روماتوئید ، سندرم شوگرن ، اسکلرودرما و تیروئیدیت هم یافت شود.
?نکته : سطوح A.M.A ممکن است در کودکان و افراد با سیستم ایمنی آسیب پذیر کمتر از حد طبیعی باشد.بعلاوه ذکر این نکته هم مهم است که سطوح A.M.A با شدت علایم مریض مبتلا به PBC و همچنین تعیین پیش آگهی برای وی ارتباطی ندارد.
نکته ای که باید بدانید :
هنگامی که سطح AMA-M2 یا AMA در خون شما بالا باشد احتمالا پزشک شما دستور به انجام بیوپسی کبد برای بررسی دقیقتر بافت کبد می دهد.در ضمن تکنیکهای عکس برداری هم ممکن است برای کشف انسداد مجاری صفراوی به کار بروند.
پرسش متداول : علت ابتلا به PBC چیست ؟
در پاسخ باید گفت علت مشخصی هنوز تععین نشده است .این بیماری نه عامل عفونی دارد نه وراثتش ارثی است، اگرچه در بعضی خانواده ها استعداد ابتلا به بیماری های خود ایمن بالاست.این بیماری میتواند در هر فرد و هر سنی رخ دهد اما نوع اولیه آن عموما در زنان میانسال وجود دارد.
منتشرشده در
مقالات
برچسبها
شنبه, 15 آبان 1400 13:05
آزمایش C-peptide
آزمایش C-peptide مشخصاً توسط کبد متابولیزه و توسط کلیه دفع و در ادرار ترشح می شود. ارتباط قوی بین سطح انسولین سرم و C-peptide وجود دارد.
C-peptide و انسولین با غلظت مولار یکسان به داخل ورید پورت ترشح میشوند ولی نسبت آنها در سرم حدود 5 به 1 تا 15 به 1 است.
تقریباً 50 درصد انسولین در عبور اولیه از کبد به سرعت برداشت میشود در حالی که برداشت کبدی C-peptide ناچیز است.از سوی دیگر در افراد سالم، نیمه عمر C-peptide و پروانسولین تقریباً 30 دقیقه است در حالی که این میزان در مورد انسولین فقط حدود 4 تا 9 دقیقه میباشد.
در حالات گرسنگی نسبت مولار C-peptide به انسولین در افراد طبیعی 5 میباشد. C-peptide را در ادرار هم میتوان اندازه گیری کرد ولی اهمیت بالینی چندانی ندارد. تست سرکوب C-peptide براساس سرکوب شدن ترشح سلولهای بتا پانکراس در طی هیپوگلیسمی است که در بیماران مبتلا به انسولینوما نسبت به افراد طبیعی این سرکوب شدن با درجه کمتری اتفاق می افتد.
علت انجام آزمایش C-peptide چیست؟
آزمایش C-peptideبه دلایل زیر انجام می شود:
تشخیص دیابت نوع ۱ از نوع ۲
بررسی علت کاهش قند خون (هیپوگلایسمی)
بررسی وضعیت تومور انسولینما

آمادگی بیمار :
معمولا برای انجام این آزمایش باید به مدت 8 ساعت ناشتا بود.
مصرف انسولین و داروهای خوراکی برای درمان دیابت نوع 2 می تواند نتیجه آزمایش را تغییر دهد.
از پزشک خود در مورد قطع کردن مصرف داروهای خود سوال کنید.
با پزشک خود در مورد نگرانی که در مورد آزمایش دارید صحبت کنید٬ احتمال خطر آن ٬نحوه انجام آزمایش یا نتایج احتمالی آزمایش. این کار به شما کمک می کند که اهمیت این آزمایش را متوجه شوید٬ (پر کردن فرم اطلاعات پزشکی).
تست های تکمیلی :
InsulinوGlucose
منتشرشده در
مقالات
برچسبها